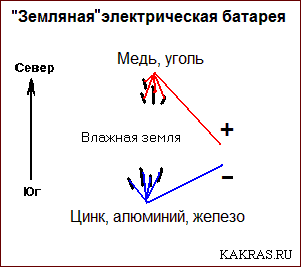
Земляная электрическая батарея
Самодельный «земляной» гальванический (электролитический) элемент делается из имеющихся материалов, с выбором по максимальной разности их электродных потенциалов (напряжение, в режиме холостого хода, между медной и цинковой пластиной – порядка 1 вольта, см. таблицу 1). Это могут быть старые железные трубы и листы оцинкованного железа, угольная куча или древесная зола, моток алюминиевого провода и проч. Сгодится любой металлолом – жестянки, металлические конструкции и т.д. Работать такая батарея может долго – месяцы (до зимних холодов, когда верхний слой почвы леденеет и становится почти диэлектриком). Быстрее корродирует (разрушается растворяясь) – минусовой электрод.
Мощность зависит от конструкции, геометрических линейных размеров, физико-химических свойств грунта и применяемого материала. Наивысший К.П.Д. одного небольшого элемента, под нагрузкой – достигается при токе 1 – 5 миллиампер, при напряжении в десятые доли вольта.
C2H6 + H2O Eo = +0.46 —>
«Ряд напряжений металлов» (электрохимический ряд стандартных
окислительно-восстановительных потенциалов), вольт:
K (Калий) = -2,9
Na (Натрий) = -2,71
Mg (Магний) = -2,36
Al (Алюминий) = -1,66
Mn (Марганец) = -1,2
Zn (Цинк) = -0,76
Fe (Железо, сталь)
= -0,4
Ni (Никель) = -0,25
Sn (Олово) = -0,14
Pb (Свинец) = -0,13
Бронза
= 0
Cu (Медь) = +0,34
С (Графит, каменный уголь, древесная зола)
= +0,4 (?)
Ag (Серебро) = +0,8
Au (Золото) = +1,50
// Графит – имеет, как и металлы, электронную проводимость. Его электродный потенциал довольно высок, имея значение, приблизительно +0,4 вольт (эта величина зависит от многих физико-химических факторов). Если нет электротехнического чистого графита, приблизительным эквивалентом, заменой ему – будет обычный каменный уголь, применяемый в печном отоплении или металлургический кокс. Электродом послужит и обычная угольная куча (или печная зола, пепел), с вылитой на неё водой (сухой, молотый в крошку уголь – очень плохо проводит электричество). В качестве токоотводов – медные листы или трубы, моток ненужной стальной или алюминиевой проволоки и прочего лома металла.
От земляной батареи можно запитать, при подключении через преобразователь – например, радиоприемник.
Оба электрода помещают (забивают трубу / штырь или закапывают пластину и прочее) во влажный грунт (в качестве электролита гальванического элемента) на глубину 1-2 м (то есть, ниже глубины промерзания почвы в зимнее время, для данного района, если делаете всесезонный девайс), на расстоянии от полуметра до нескольких метров, друг от друга. Для уменьшения электрического сопротивления в межэлектродном пространстве (это увеличит ток) – его надо полить водой. На минусовой, цинковый электрод – вылить раствор поваренной соли (NaCl) или щёлочь (К или Na).
Подходящие гальванические пары: медь и/или уголь – будут положительным электродом земляного элемента, а цинк, алюминий или железо (в том числе, оцинкованное) – отрицательным (его вывод (алюминиевый провод) надо изолировать от земли). Места соединений – герметизируются (покрыть защитной водостойкой краской, лаком или битумной мастикой).
Поверхность алюмишки быстро окисляется, поэтому алюминиевый стержень, периодически, подбивается кувалдой (при этом – абразивные частицы грунта, частично, сдирают окисную плёнку). Если верхушки электродов расположены над землёй – к ним подключаются (надёжной скруткой или на винтовое соединение) любым изолированным проводом или проволокой, зачистив, предварительно, контактные поверхности отводов.
Для получения электрического напряжения, в несколько раз больше 1 вольта – собираются батареи из нескольких элементов, соединённых последовательно. Для увеличения силы тока – их соединяют параллельно, увеличивают рабочую площадь электродов и поливают водой (с растворённой солью или с разведённой печной золой) землю между электродами. Концентрированный (большой плотности) электролит или морскую воду – нельзя выливать на землю (иначе, там ничего не будет расти).
Положительный электрод (медный/угольный, должен быть глубже, чем южный) – на северной точке (если линия ориентирована вдоль магнитного меридиана), отрицательный – находится южнее. К цинковой пластине – приложить слой войлока.
// Удельное электрическое сопротивление обычной питьевой воды, довольно мало – до первых десятков Ом•м. В солончаках – на один-два порядка меньше (из-за высокой степени ионной проводимости). Влажная почва – действует как электролит в гальваническом элементе.
Обычно, на практике – применяют комбинированный, последовательнопараллельный способ соединения. Этого бывает достаточно для питания радио-приёмника.
Гальванический элемент можно собрать и в миниатюре – в стеклянную банку, с электролитом в виде 20%-го раствора поваренной соли (или 5%-й уксус), помещаются две пластины из электротехнической меди и цынка (или железа). Под нагрузкой, на положительных пластинах выделяются газовые пузырьки (водород), отчего, во время работы, и уменьшается ток. Дря решения этой проблемы – плюсовой электрод окружают деполяризатором, состоящим из равных частей порошка (помещается в холщовый мешок) графита и пиролюзита.
Фруктово-овощные («зелёные», экологичные) источники электрического тока
В плоды растений, в свежий лимон, в яблоко или в отварной картофель, втыкаются металлические электроды, например – железный гвоздь и зачищенный медный провод. Напряжение на элементе – может достигать 1 вольта. Ток – до нескольких миллиампер.
Батарея – получится при соединении нескольких таких элементов. Её, может быть, и хватит для питания светодиода.
Экзотические девайсы
Гальванические пары используются во множестве устройств, в том числе и, в так называемых, «Цилиндрах Фараона» (Жезлы Гора, применяемые в эзотерических практиках, в виде цилиндров из меди и цинка, длиной 15 сантиметров, диаметром 2.5-3 см., с ферритовым и угольным наполнителем). Их, определёнными способами, держат одновременно в двух руках. При соединении – появляется дополнительный ток в замкнутой, телом, электрической цепи. Медный электрод (с правой стороны) – имеет полярность со знаком «плюс».
Свободная энергия от электромагнитного излучения мощных передающих радиостанций
Об этом уже и так много написано, в том числе – в статьях, в журнальных публикациях и книгах В.Полякова.
Наводимая, электромагнитным полем широковещательной станции, ЭДС и ток – могут составить, примерно, 1 вольт и до нескольких сотен микроампер. Это – вблизи крупных городов (на расстоянии до 100 км.), при хорошем заземлении антенны и нормальной погоде (когда нет, поблизости, опасной грозы).
В случае катастрофического природного, военного или техногенного Апокалипсиса (БП) – данная технология почти не будет работать, т.к. останется только излучение от ближайших грозовых разрядов, а многие мощные радиотрансляторы прекратят вещание.
Как добыть бесплатное электричество в экстремальных условиях. Химические источники тока (гальванические элементы).
Free energy from the earth («земляная электрическая батарея»). Минисправочник по некоторым видам источников электроэнергии и их параметрам.
Источник
ГАЛЬВАНИЧЕСКИЕ ЭЛЕМЕНТЫ: САМОДЕЛЬНАЯ БАТАРЕЯ
Каждому из нас знакомы химические источники тока различных типов и форм. Но как это часто случается, мы редко задумываемся о том, как устроен этот совершенно привычный и обыденный предмет. А между тем, появление первых химических источников тока, положило начало превращению электричества из лабораторной диковинки в нашего повседневного помощника.
В 1790 г. итальянский физиолог Луиджи Гальвани заметил, что лапка препарированной лягушки дергается, если к ней одновременно прикоснуться двумя инструментами из разных металлов. В то время уже было известно, что мышцы могут сокращаться под действием электрического тока, так, что Гальвани правильно приписал это явление действию электрического тока. Правда, он считал, что электрический ток появляется благодаря каким-то физиологическим процессам в лапке лягушки.
Правильное объяснение этому явлению смог дать другой итальянский ученый Алессандро Вольта. Он установил, что это явление связано с наличием двух разнородных металлов, соприкасающихся с электролитом, в роли которого выступала кровь лягушки, а сама лапка играла лишь роль чувствительного индикатора электрического тока [1]. Опираясь на свои исследования Вольта в 1799г. создал первый химический источник тока. В этом устройстве Вольта использовал медный и цинковый электроды, погруженные в раствор серной кислоты.
Цинк бурно реагирует с кислотами. В раствор переходят не атомы цинка, а положительные ионы, так что в электроде остается избыток электронов, следовательно, цинковая пластина заряжается отрицательно. Вообще, большинство металлов при погружении в электролит заряжается отрицательно, на поверхности медной пластинки протекает подобный процесс. Но избыток отрицательных зарядов на медном электроде гораздо меньше, а значит, относительно цинкового электрода его потенциал получается более высоким. Если соединить внешним проводником медную и цинковую пластины, то электроны начнут перемещаться с цинковой пластины на медную, т.е. в цепи потечет электрический ток [2].
Электрическое напряжение, возникающее между электродами, зависит от того, из каких металлов изготовлены электроды и от их взаимодействия с электролитом. Напряжение, даваемое элементом, никак не зависит от площади пластин.
Часто напряжения, даваемого одним гальваническим элементом, недостаточно. Тогда их можно соединять последовательно в батареи.
Вообще изготовить химический источник тока совсем нетрудно: надо поместить в электролит две пластинки из разных металлов [3]. Такие гальванические элементы возникают самопроизвольно. Например, намочил дождь крышу, покрытую оцинкованным железом, на железе наверняка имеются царапины, так, что и железо, и цинк вступили в контакт с водой, которая играет роль электролита. Цинк в такой паре начнёт активно разрушаться, а вот железо не пострадает, пока не разрушится весь цинк. Именно для этого и покрывают железо слоем цинка.
По той же самой причине скручивать вместе медные и алюминиевые провода, это, мягко говоря, не самая лучшая идея. В месте контакта начнется гальваническая коррозия, которая приведет к росту электрического сопротивления контакта, что в свою очередь приведет к большему выделению тепла и еще более быстрой коррозии. Все вместе это может стать причиной разрушения соединения и даже пожара.
Нагляднее всего можно пронаблюдать гальваническую коррозию на примере контактов железа с цинком и медью в растворе соли. Железные скрепки были надеты на цинковую и медную пластины и погружены в раствор соли.
Через сутки скрепка, соединенная с медной пластиной, покрылась ржавчиной. В то время, как скрепка, бывшая в контакте с цинком, совершенно не пострадала.
Ученые составили электрохимический ряд напряжений металлов. Чем дальше друг от друга отстоят металлы в этом ряду, тем более высокое напряжение дает гальванический элемент, составленный из этих металлов. Так пара золото – литий теоретически может дать электродвижущую силу (ЭДС) 4,72 В. Но такая пара в водной среде работать не сможет – литий это щелочной металл, легко реагирующий с водой, а золото стоит слишком дорого для подобного применения.
На практике элемент Вольта обладает рядом серьёзных недостатков.
- Во-первых, электролитом ему служит весьма едкая жидкость – раствор серной кислоты. Жидкий электролит всегда представляет собой неудобство или даже опасность. Он может расплескаться, разлиться при повреждении корпуса.
- Во-вторых, на медном электроде такого элемента будет выделяться водород. Это явление называется поляризацией. По многим свойствам водород весьма близок к металлам, так что его пузырьки создадут дополнительную ЭДС поляризации, стремящейся вызвать ток противоположного направления [2]. Кроме того, пузырьки газа не пропускают электрический ток, что тоже ведет к ослаблению тока. Поэтому приходится периодически встряхивать сосуд, удаляя пузырьки механически, или вводя в состав электролита специальные деполяризаторы.
- В третьих, в процессе работы гальванического элемента Вольта, цинковый электрод постепенно растворяется. Теоретически, когда гальванический элемент не используют, разрушение цинкового электрода должно прекратиться, но поскольку почти всегда в составе цинка есть примеси других металлов, они при соприкосновении с электролитом играют роль второго электрода, образуя короткозамкнутый элемент, что ведет к гальванической коррозии цинкового электрода [2]. Для того, чтобы устранить этот недостаток, приходится использовать сверхчистый цинк или конструктивно предусматривать возможность извлечения цинкового электрода из электролита. Так что когда батарея не используется, электролит из нее следует сливать.
Но для демонстрационных целей всеми этими недостатками можно пренебречь, если заменить серную кислоту более безопасным электролитом.
Изготовление батарейки
При изготовлении демонстрационной батареи гальванических элементов будем использовать стандартную пару – медь и цинк. Медную фольгу можно найти в некоторых трансформаторах. В крайнем случае, можно сделать медный электрод из свернутой в спираль голой медной проволоки [4]. Цинк можно добыть из разрядившихся солевых элементов питания, как правило, в них остается достаточно много металлического цинка даже, когда элемент непригоден к дальнейшему использованию. Вместо раствора кислоты, возьмем 10% раствор поваренной соли. В качестве емкости для электролита взяты пластиковые емкости от витаминов объемом примерно 50-100 мл.
В качестве контактов использованы винты, которые одновременно закрепляю электроды на крышке. При этом крайне желательно крепить медные электроды латунным винтом. Цинковую пластину можно без проблем крепить стальным винтом. Для герметизации под гайку подложена подходящая по размеру резиновая сантехническая прокладка.
Батарея из трех гальванических элементов позволяет питать светодиод.
Напряжение на одном элементе батареи составляет около 1 В.
Ток, отдаваемый в нагрузку, составляет около 0,23 мА
Такого тока достаточно для свечения светодиода. Однако на фотографии это свечение можно заметить, только если снимать при большой светочувствительности.
Такую батарею можно использовать в школе, например для выполнения лабораторной работы, по определению внутреннего сопротивления источника тока [5].
Источник