- Изготовление простейшего гальванического элемента
- Принцип действия
- История развития конструкции элемента Вольта
- Вторая половина девятнадцатого века
- Современность
- Изготовление долгосрочного элемента питания для портативных устройств
- Необходимые материалы
- Сборка конструкции химического источника электроэнергии
- Технология изготовления альтернативного источника питания
- Digitrode
- цифровая электроника вычислительная техника встраиваемые системы
- Как сделать батарейку 9 В своими руками
- Форум самодельщиков: Батерейка из монеток, или Вольтов столб — Форум самодельщиков
- Батерейка из монеток, или Вольтов столб интересный опыт, хотя и малополезный
- #1 MityaKiller
- Изготовление лабораторной батареи гальванических элементов, вместе с ребёнком
Изготовление простейшего гальванического элемента
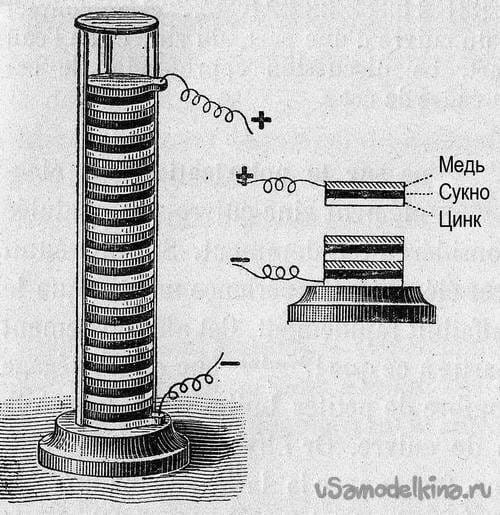
Вольтов столб был изобретён таким известным учёным из Италии, как Алессандр Вольт. Он провел первые испытания химического источника тока еще в 1800 году. Его назвали элементом Вольта. Он представлял собой сосуд с подсоленной водой и опущенными в неё цинковыми и медными пластинами, которые соединялись проволокой. Потом учёный собрал целую батарею из таких элементов, которая позже была названа Вольтовым столбом. Вольтов столб своими руками могли сделать любые испытатели и с успехом применяли его.
Принцип действия
Наипростейший медно-цинковый столб собирается из 2 электродных пластин, расположенных в растворе электролита. В этом случае, погружая электролит в пространство между металлами, Вы создаете разницу потенциалов.
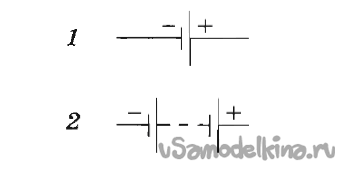
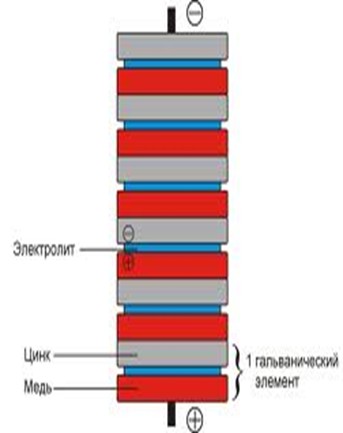
Для создания более высокого напряжения или мощности этих элементов заводские батарейки делают в виде последовательно соединённых, количество увеличивают до того, как получат нужное напряжение.
Заводская схема конструкции
История развития конструкции элемента Вольта
Открытие получило развитие в использовании учёных из других стран, которые его успешно применяли в своих исследованиях. К примеру, в 1802 году академик из России Петров собрал батарею — Вольтов столб из 2,1 тыс. элементов, которая обеспечивала электрическую дугу.
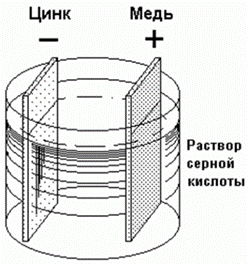
В дальнейшем, в 1836 году, химик Дж. Дэниель английского происхождения модернизировал элемент Вольта за счет того, что поместил электроды из цинка и меди в раствор из серной кислоты. Такую конструкцию прозвали как устройство вольтова столба.
Вторая половина девятнадцатого века
Затем в 1859 году во Франции исследователь физических явлений Гастон Планте изобрёл другой тип аккумулятора — свинцово-кислотный. Он до сих пор используется в автомобильных аккумуляторах. Но уже в 1865 году Ж. Лекланше изобрел свой гальванический элемент, который назвали элемент Лекланше. Он состоял из цинкового стакана, который был заполнен раствором водного хлористого аммония или другой соли хлора. В него помещали агломерат из оксида (IV)марганца с формулой — MnO2 с угольным токоотводом.
Модификация этой конструкции может использоваться и в современных солевых батарейках в различных бытовых устройствах. В это время в 1890 году в городе Нью-Йорк исследователь Конрад Губерт, который иммигрировал из России, создал 1-й электрический фонарик. Далее компания National Carbon в 1896 году начинает массовое производство первых сухих элементов имени Лекланше «Columbia» в мире. Самый наибольшее прослужившее гальваническое устройство на серно-цинковой батарее – накопитель, изготовленный в Лондоне во второй половине 19-го года. Он был подключён к звонку и до сих пор работает.
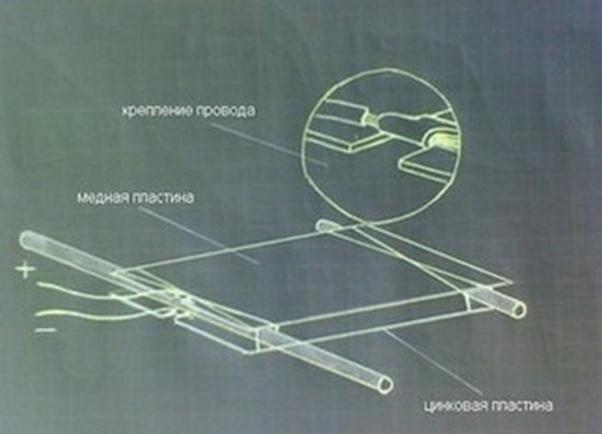
Стандартная схема простейшей батарейки
Современность
Портативной технике, которой пользуется человек сегодня, необходимо напряжение как минимум в 3,6 вольта (но лучше — 4,5). Для получения такого показателя рекомендуется использовать 4-5 выше описанных элементов, соединенных последовательно. Когда соединяют 5 литровых (объём электролита) элементов, то добиваются показателя в 3,5-4,6 вольт, при чем ёмкость возрастает до 45-50 ампер в час. Если разряд тока достигнет 400-600 миллиампер в час, то Вы сможете питать такой батарейкой небольшой радиоприемник или фонарик светодиодного типа. Также можно обеспечить зарядкой миниатюрный аккумулятор телефона до 10-20 часов, но питание современных телефонов и гаджетов потребует более серьезных источников.
Изготовление долгосрочного элемента питания для портативных устройств
Необходимые материалы
Чтобы самостоятельно сделать вольтов столб (химический источник электроэнергии), Вам понадобится:
- ёмкость побольше, например, объемом 40-50 литров (это минимум для стабильного питания портативных светодиодных лампочек и другой техники).
- пять медных пластин 20/40;
- пять цинковых пластин 20/40;
- любая соль.
На подготовительном этапе каждую пластинку припаивают или запрессовывают, загибая уголки пластин. Затем вставляют проводок и заплющивают молотком.
Сборка конструкции химического источника электроэнергии
Закрепите между собой пластины через электронопроводящие прокладки. Для этого подойдут деревянные брусочки или пластмассовые трубки. Опустите столб пластин в ёмкость с электролитом (раствор поваренной соли, нашатыря или серной кислоты — автоэлектролит). Кислоту добавляют порциями и периодически проверяют плотность раствора аэрометром. Необходимо добиться, чтобы она составляла 1,21-1,31 грамм на см3 – это приблизительно 280-300 г кислоты.
Модель одного элемента
Далее соедините получившиеся батарейки: медные пластины одного проводком соедините с цинковой полоской второго элемента. Таким образом, у Вас получится с одной стороны блока — медная полоска закреплена с проводом (+ положительная), а с противоположной — цинковая (отрицательная). Эффективность такого источника можно повысить за счет увеличения площади пластин, или использования более сильного электролита (серной кислоты).
Технология изготовления альтернативного источника питания
Источник
Digitrode
цифровая электроника вычислительная техника встраиваемые системы
Как сделать батарейку 9 В своими руками
Вольтов столб представлял собой первую в мире гальваническую батарею, которая была немного больше, чем серебряные и цинковые диски, разделенные бумагой, пропитанной соленой водой. Зачастую в учебных классах проводится эксперимент по сборке такого столба из кучи медных монет, оловянной фольги и уксуса или лимонного сока.
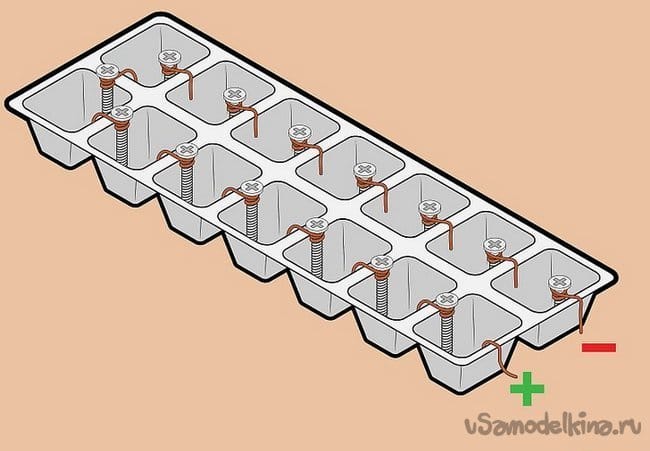
Энтузиаст Omars2 имеет другой подход к этому старому эксперименту. Он разработал методику создания батарейки на напряжение 9 В с использованием некоторого количества винтов из цинка, медной проволоки и соленой воды.
Поршень шприца в данном случае служит в качестве подложки для гальванических ячеек, и каждая ячейка представляет собой только винт с обернутой вокруг него бумагой. При этом после его обворачивания бумагой на него наматывают медную проволоку, всего получается 35 витков. Батарея пропитана соленой водой, впрочем, скорее всего, уксус или лимонный сок будут работать еще лучше. Нагревание электролита также является хорошей идеей.
Принцип действия такой самодельной батареи довольно прост. Соль растворяется в положительно заряженных ионах натрия и отрицательно заряженных атомах хлора с образованием электролита. Катод отдает электроны в раствор, оставляя его положительным. Другой электрод, носящий название анод, собирает электроны, поэтому он имеет только отрицательный заряд. Разница между величинами зарядов на двух электродах создает разность потенциалов, то есть напряжение. Когда вы замыкаете контур, электроны перетекают из анода обратно в катод, вызывая протекание электрического тока.
Собрав такую батарею и подключив к ней мультиеметр, можно ожидать, что показание напряжения будет в районе от 7 В до 9 В постоянного тока, если все, конечно, было сделано правильно. После этого к такой батареи можно подключить некоторую нагрузку, например, лампочку,, и она должна работать нормально. Чтобы зарядить эту батарею, вам понадобится мультиметр, чтобы определить полярность этой батареи, а затем вам потребуется использовать 9-вольтовый адаптер постоянного тока для зарядки. Выход должен быть где-то около 0.30 — 0.40 A.
Процесс создания батареи 9V показан на видео ниже.
Если вы предпочтете сделать эту версию с монетами, то следите за тем, чтобы они все содержали большое количество меди. В противном случае такая батарея либо будет работать слабо, либо не будет работать совсем. При отсутствии медных монет вам понадобится другой металлический материал, например, оловянная фольга.
Источник
Форум самодельщиков: Батерейка из монеток, или Вольтов столб — Форум самодельщиков
- Правила форума
- Просмотр новых публикаций
Пройдя короткую регистрацию , вы сможете создавать и комментировать темы, зарабатывать репутацию, отправлять личные сообщения и многое другое!
Батерейка из монеток, или Вольтов столб интересный опыт, хотя и малополезный
- 2 Страниц
- 1
- 2
- →
- Вы не можете создать новую тему
- Вы не можете ответить в тему
#1  MityaKiller
MityaKiller
- Изобретатель
- Группа: Пользователи
- Сообщений: 455
- Регистрация: 31 August 10
В общем, нам понадобится :
1)Собственно монетки, обязательно медные(российские 50 и 10 копеек)!
2)Уксус или сильно солёная вода ( электролит короче )
3)Алюминиевая фольга
4)Бумажка (хотя это не обязательно)
Начнём!
Для начала смотрим, чтобы монетки не были засранными, в противном случае их придётся мыть. Берём бумажку, и режем на квадратики так, чтобы ими можно было закрыть монетку. Вымачиваем полученные бумажки в электролите. Далее начинаем строить батарейку. Складываем компоненты по схеме монетка — бумажка — кусочек фольги — монетка — бумажка — кусочек фольги — . и т.д. Делаем, пока не закончится терпение/фольга/монетки/электролит
Когда что-либо закончится, берём мультиметр и меряем напряжение. У меня вышло максимум 18 вольт (на фотке 15 вольт). Вот собственно и всё. Схему мне такой батарейкой запитать не удалось, видимо заряд маленький. Ну и собственно фотки:
Источник
Изготовление лабораторной батареи гальванических элементов, вместе с ребёнком
Простые технические эксперименты очень полезно делать с детьми, это и совместное времяпровождение, и прививание навыков, и понимание маленькими конструкторами, основ, того, что батоны, как в известном мультике, не на деревьях растут.
В этот раз, мы решили сделать простейший химический источник тока, и попытаться его применить для чего ни будь практического. Говоря о практическом применении, стоит вспомнить, что всего несколько поколений назад, радиолюбителям, для питания их батарейных радиоприемников и усилителей, предлагались к самостоятельному изготовлению несколько типов гальванических элементов или аккумуляторов. Это элементы Лекланше и Попова [1] стр. 9…18, или свинцово-поташный или газовый аккумулятор [1], стр. 22…28. Несколько, относительно сильноточных элементов соединяли в батарею накаливания (нити накаливания радиоламп), десятки элементов поменьше, в анодную батарею, напряжение которой, могло достигать 60-80 вольт. Батареи были «мокрыми» — с жидким электролитом и требовали ухода и обслуживания.
Итак, гальванический элемент, несколько слов «как?» и «почему?». Электрический ток возникает при взаимодействии разных металлов. При этом возникает различная разность потенциалов (напряжение). Еще в 1793 году Алессандро Вольта, конструируя гальванический элемент (Вольтов столб), установил относительную активность известных тогда металлов: Zn, Pb, Sn, Fe, Cu, Ag, Au. «Сила» гальванического элемента оказывалась тем больше, чем дальше стояли друг от друга металлы в этом ряду (ряд напряжений).
Позже, для упорядочивания данных, приняли за ноль отсчета потенциал «водородного электрода». Измерив потенциал металлов в паре с ним, расположили подопытные металлы в ряд. Полученная таблица получила название «Электрохимический ряд напряжений металлов» и в кабинете химии, обязана висеть рядом с периодической системой и портретом Дмитрия Ивановича.
Ряд напряжений металлов – полезнейшая штуковина, в нашем случае, мы, как и Алессандро Вольта, будем знать – чем дальше металлы отстоят друг от друга, тем большее напряжение удастся получить.
В своих опытах, как и классики, мы использовали медь и цинк. При погружении пластинок в электролит, между ним и цинковой пластинкой, происходит химическая реакция, в результате которой на пластинке скапливаются отрицательные заряды и она заряжается отрицательно. В результате реакции происходящей в гальваническом элементе, цинковый электрод постепенно растворяется.
На медном электроде, при работе гальванического элемента, образуются мельчайшие пузырьки водорода, изолирующие поверхность меди от электролита. Явление называется газовой поляризацией, в гальваническом элементе оно вредно, с ним борются. Для удаления выделяющегося водорода, в электролит вводятся вещества связывающие водород, называемые деполяризаторами. В их роли часто выступают соединения марганца, медный купорос. В простых опытах, можно применить аптечный перманганат калия.
Что мы использовали для эксперимента.
Приборы и материалы.
Для сборки гальванических элементов, в качестве медных электродов, можно использовать проволоку, провод, фольгу. Цинк можно извлечь из сухих элементов, применить оцинкованные изделия. Вместо цинкового, можно попробовать применить электрод из алюминия или железа. Поваренная соль для электролита, немного мягкого монтажного провода. Непременно нужен вольтметр или мультиметр, кусачки, ножницы. В качестве сосудов, можно применять неметаллические емкости подходящего размера. Стеклянные, удобнее легких пластиковых стаканчиков – они тяжелее, устойчивее, опрокинуть их труднее. Очень хорошо, если найдется слаботочная низковольтная нагрузка – простое радио, кварцевые часы, и т.п.
«Высоковольтная» батарея из проволоки и саморезов.
Прельстившись простотой деталей, и относительно высоким получаемым напряжением, мы попытались собрать такую батарею. Здесь применяется «классическая» пара металлов – медь-цинк. Идея состоит в применении в качестве цинкового электрода, оцинкованного крепежа. Изящно. Понятно, что на длительную работу, такой элемент не рассчитан – тонкий слой цинка быстро растворится, однако, для кратковременного эксперимента это и не важно. Зато оцинкованных шурупов или винтиков везде полно.
В качестве медного электрода применена проволока – также, широко доступный материал, кроме того – удобнейший монтаж элементов в батарею – все элементы соединены последовательно – плюс одного к минусу следующего. При этом напряжение суммируется, ток остается прежним.
После подбора необходимого количества оцинкованного крепежа нужной длины, мы нашли подходящую медную проволочку. Это обмоточный провод в лаковой изоляции. Диаметр провода около 0,5 мм.
Полюшка зачищает лаковую изоляцию, несколько раз, с усилием протягивая провод, через сложенную вдвое шлифовальную шкурку средней крупности.

Затем, подготавливает пары электродиков – под шляпкой самореза, плотно наматывает два-три витка проволоки и обрезает лишнее.
Сборка батареи – в качестве емкости использовано корытце для замораживания льда. Можно применить и ячейки от коробочных конфет, правда, они понежнее. После установки электродов на стенках между ячейками, заполняем емкости электролитом. Мы использовали раствор поваренной соли – столовую ложку с горкой на 0,5 л теплой воды. Для заполнения очень удобно применять медицинскую спринцовку.
— Очень хочется произвести на вас приятное впечатление.
— Вам это удалось… уже.
— Усилить хочется.
Мы нашли еще несколько шурупов для электродов и добавили элементов в батарее, вот, что у нас получилось. Напряжение на высокоомной нагрузке (входное сопротивление цифрового вольтметра) изрядное, но на любой, сколь ни будь заметной нагрузке, сильно падает.
Попытаемся сделать аналогичный гальванический элемент (батарею) с электродами побольше.
В качестве емкости, мы применили поллитровую баночку (две), в нее поместятся пластинки значительной площади. В качестве электродов мы взяли тонкую медную фольгу и цинк – остатки стаканчика от фабричного «сухого» элемента, разобранного при добыче графита для огнеупорной обмазки.
Остатки засохших кристаллических солей мы счистили проволочной щеткой и вырезали большими ножницами две пластинки, примерно равной площади. Из медной фольги, вырезали две соответствующих полосочки. Тоже ножницами. Получили две пары электродов, которыми снарядили наши элементы, не мудрствуя, загнув их края на горлышке банки.
В емкости побольше, приготовили электролит – поваренную соль, растворили в теплой воде, концентрация та же, и залили подготовленные элементы.
Два элемента мы соединили последовательно, при помощи кусочка монтажного провода и двух зажимов «крокодил». Та-ак, прекрасно, напряжение батареи близко к стандартному «пальчиковому», попробуем использовать. Один элемент напряжением 1.5 В используется в электромеханических часах, кроме того, ток потребления часов очень мал и наша батарея вполне сможет его осилить.
Из часов мы извлекли штатный элемент питания и к клеммам присоединили по кусочку монтажного провода. Соблюдая полярность (медная пластинка – «+», цинковая – «-»), подключили наши часы к самодельной батарее, вуаля! Часы работают, напряжение «проседает» до 1,3 В. Часы, преотлично работали несколько часов, пока мы всем не похвастались (однако колдун!) потом надоело.
Внутреняя конституция у любого ребенка такова, что внимание на одном предмете, он способен сосредотачивать не более 15…20 минут, и все занятия с детьми следует планировать так, чтобы они укладывались в это время, либо переключаться между разными занятиями, иначе оба намучаетесь.
В качестве нагрузки, лучше применить, что ни будь движущееся или светящееся – цифры на вольтметре впечатляют ум, но не сердце. Кроме часов и калькуляторов, наверняка вызовет восхищение, работа от самодельной батареи небольшого радиоприемника (как вариант — самодельного!).
При долговременном использовании, электролит элементов стоит предохранить от пыли и испарения, и позаботиться о деполяризаторе — ну, хотя бы закупорив баночку обрезком полиэтиленовой пленки с резинкой и добавив в электролит перманганат калия. Более того, лучше сразу собирать помянутый элемент Попова.
Кроме оцинкованных саморезов, можно применить оцинкованную листовую сталь, для крупных элементов это удобнее — на время эксперимента можно получить значительный ток и запитать что ни будь (пошевелив пальцами в воздухе) этакое.
Список используемой литературы.
1. П.Стрелков. Знай и умей. Пионер-электротехник. Детгиз. 1960 г.
2. В.С.Полосин, В.Г.Прокопенко. Практикум по методике преподавания химии. Москва, «Просвещение», 1989 г. Стр.202,203.
Источник





 MityaKiller
MityaKiller